- + Merck Millipore
- + Thermo Fisher
- + IKA
- + 顯微鏡
- + 光度計
- + 成像系統(tǒng)
- + MACS Miltenyi
- + 均質(zhì)機
- + 粒子計數(shù)器
- + 凍干機
- + 滅菌系統(tǒng)
- + 細胞
- + 微量移液工作站
- + 振蕩培養(yǎng)箱
- + 生物反應器
- + 切片機
- + 培養(yǎng)箱
- + 蠕動泵
- + 細胞破(粉)碎機
- + 轉印膜
- + 超濾管
- + Pellicon 超濾系統(tǒng)
- + 超低溫冰箱
- + 清洗機
- + 干燥機
- + 洗瓶機
- + 離心泵
- + 容積泵
- + 各種閥
- + 酶標儀
- + 洗衣板
- + 旋光儀
- + 折光儀
- + 行星球磨機
- + 振動篩
- + 基因導入儀
- + 手套系列
- + 接頭\\連接器
- + 培養(yǎng)板/培養(yǎng)瓶
- + 溫度控制系統(tǒng)
- + 制冷器
- + 存取系統(tǒng)
- + 軋蓋機
- + 細胞因子
- + 細胞分選儀
- + 生物安全柜
- + 滲透壓儀
- + 拉曼光譜儀
- + 電泳系統(tǒng)
- + 純水系統(tǒng)
- + 萃取儀
- + 譜新生物
- + TA 儀器
- + wako
還在為如何提取完整的外泌體發(fā)愁嗎?
更新時間:2022-04-14 瀏覽次數(shù):2482
在過去的幾十年中,外泌體因其在改變細胞功能中的作用而受到了廣泛關注。外泌體是膜結合的納米級囊泡,最初通過晚期核內(nèi)體的內(nèi)陷形成為特定的腔內(nèi)囊泡群。由于晚期多泡內(nèi)體與質(zhì)膜融合,這些內(nèi)體來源的腔內(nèi)囊泡隨后被釋放到細胞外環(huán)境中,這是一種將它們與其他類型的細胞外囊泡區(qū)分開來的生物發(fā)生機制[1]。
因此,外泌體外膜由富含供體細胞膜衍生蛋白的磷脂雙層和繼承細胞質(zhì)生物分子(包括蛋白質(zhì)、酶、mRNA、miRNA 和代謝物)的水內(nèi)核組成。外泌體的大小在 20-120 nm 之間,并且在形態(tài)和結構上因親代細胞而異[2]。外泌體亞群呈現(xiàn)出不同的形狀,從球形到絲狀和細長形,還可以包括不同的子隔室[3]。

外泌體結構及形成過程
目前,已經(jīng)開發(fā)了多種分離策略來從各種生物來源中離外泌體,這些生物來源包括牛奶、血液和尿液,以及植物衍生產(chǎn)品,例如水果和蔬菜。
外泌體利用多種內(nèi)吞機制進入細胞。有趣的是,外泌體還可以克服物種障礙,在不同來源的細胞之間傳遞生物分子[4]。外泌體介導生物功能,從而調(diào)節(jié)體內(nèi)重要的生理和病理過程[5]
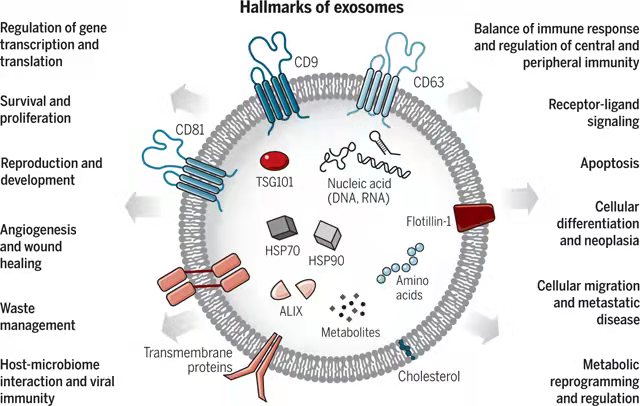
外泌體生物學功能
由于外泌體是內(nèi)源性具有生物活性的生物分子的天然載體,它們已被廣泛用于主動和被動傳遞合成生物分子。它們的內(nèi)源性和納米特性也使這些納米載體能夠跨越生物屏障,并賦予它們優(yōu)良的生物相容性[6]。
因此,這幾年各領域廣泛展開外泌體相關的研究,外泌體研究橫跨幾乎所有的研究領域(免疫、神經(jīng)系統(tǒng)、腫瘤、內(nèi)分泌、循環(huán)系統(tǒng)等)。
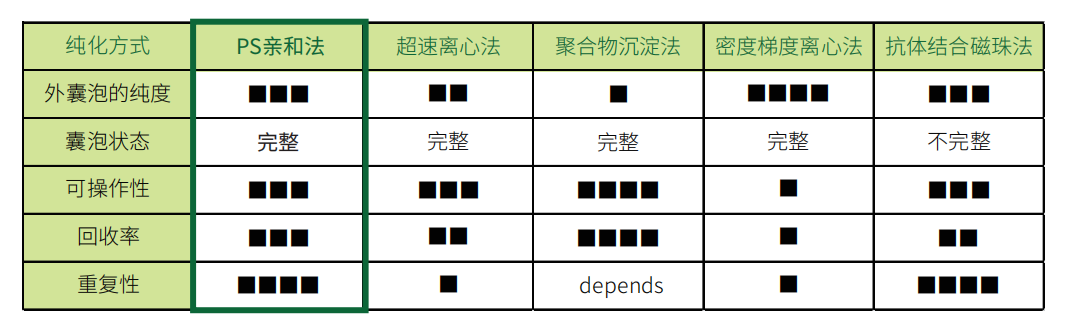
然而,目前用于外泌體研究的實驗技術仍處于開發(fā)階段,許多問題仍有待改進。例如,外泌體純化方法中,超速離心法和聚合物沉淀法(市售試劑盒)提取的外泌體中混有多種雜質(zhì),會給后續(xù)實驗造成許多障礙。而抗體親和法和密度梯度離心法這兩種提取方法的問題在于,雖然可以提取到高純度的外泌體,但外泌體結構不完整,無法用于分析外泌體的生理功能。
磷脂酰絲氨酸和Tim4新型外泌體提取法
外泌體膜雖然含有分泌細胞源蛋白質(zhì)和脂質(zhì),但目前普遍認為在活細胞中磷脂酰絲氨酸(PS)通過脂質(zhì)翻轉酶作用定位于細胞膜內(nèi)側[7]。
作為通過巨噬細胞進行細胞凋亡的吞噬受體(T-cell immunoglobulin domain and mucin domain-containing protein 4,Tim4)蛋白通過細胞外域IgV域與結合了鈣離子的PS結合[8]。
利用這一原理,Wako和金澤大學醫(yī)學系免疫學華山教授共同開發(fā)一款劃時代的外泌體提取方法,利用Tim4固化磁珠,在鈣離子存在下捕捉培養(yǎng)上清和血清等樣品中的外泌體,再添加螯合劑從而提取外泌體[9]。并且MagCapture™外泌體提取試劑盒PS實現(xiàn)了比傳統(tǒng)的外泌體純化法更加簡單地提取高純度完整狀態(tài)的外泌體。
這是迄今為止取代黃金標準超速離心法的新型外泌體純化法。
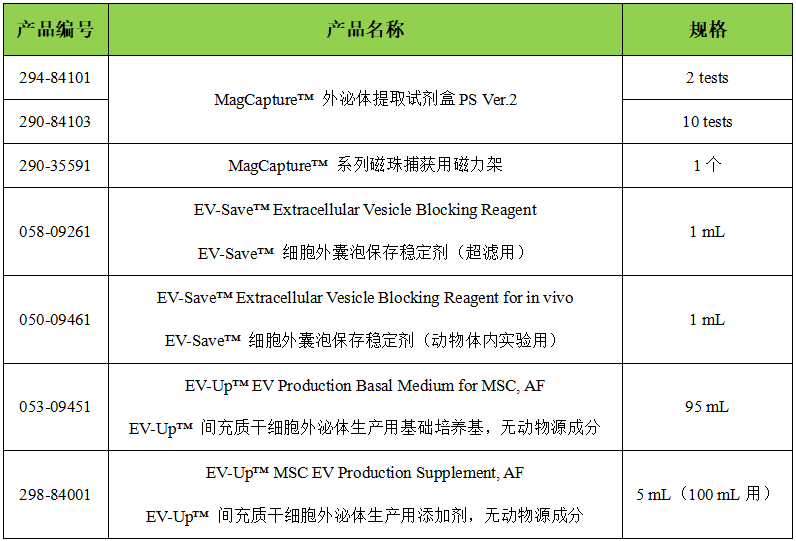
MagCapture™ 外泌體提取試劑盒PS
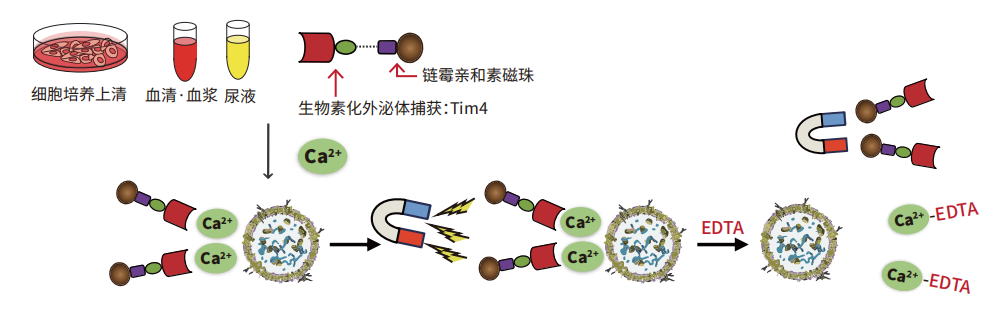
巨噬細胞表面的Tim4蛋白特異性結合細胞外囊泡表面的磷酯酰絲氨酸(PS)。
利用Tim4固化磁珠,在Ca2+ 存在條件下捕捉培養(yǎng)上清或血清等樣本中的外泌體,通過使用含有EDTA的洗脫液洗脫,可獲得高純度的完整細胞外囊泡(EVs)。
01
原理
02
特點
● 可獲得高純度完整細胞外囊泡,可用于蛋白及核酸分析、共培養(yǎng)及體內(nèi)注射
● 回收率高
● 操作簡便(3.5h),不需超速離心
03
應用實例
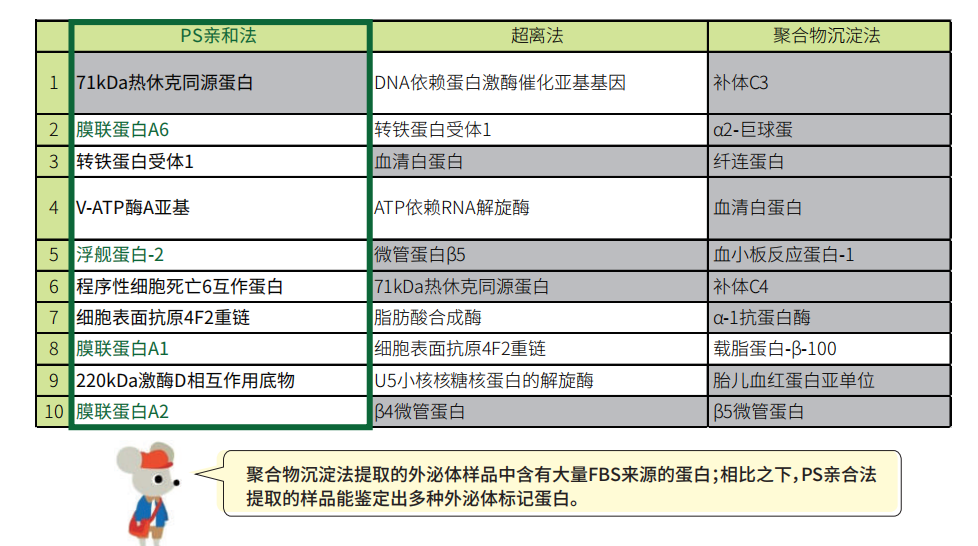
外泌體蛋白質(zhì)組學分析
通過MASS鑒定結果比較豐度最高的前 shi 種蛋白。
樣品:K562細胞培養(yǎng)上清(含10%去外泌體FBS)
白色柱:源自外囊泡的人類蛋白
灰色柱:來自FBS的牛蛋白污染物
綠色:來自外囊泡的標記蛋白
[9] Nakai Wataru.et al. (2016). A novel affinity-based method for the isolation of highly purified extracellular vesicles. Sci Rep, 6, 33935.
- (上一篇):能否用好CO2培養(yǎng)箱,在于您對其特點了解多少!
- (下一篇):如何正如何正確的選擇搖床振幅?